新闻资讯

近日,上海市第一人民医院骨肿瘤科团队在精准肿瘤医学期刊《NPJ Precision Oncology》发表题为"Targeting high-risk MYC-overexpressed osteosarcoma with an Aurora kinase inhibitor: results from a pilot umbrella trial"的重要研究成果。该研究基于团队前期建立的上海市一骨肉瘤分子分型体系,开展了针对难治性转移性骨肉瘤的精准分型伞式临床试验。
研究聚焦临床预后最差的MYC驱动型骨肉瘤亚型,完成了从基础到临床的转化研究:通过临床前实验证实了Aurora激酶抑制剂Tinengotinib对该亚型的显著抑制作用,并成功完成临床试验探索。并且,研究团队通过对上海市一骨肉瘤队列(SGH-OS Cohort)多组学测序数据分析,进一步解析了MYC驱动型骨肉瘤独特的免疫抑制微环境特征,为后续联合免疫治疗提供了重要的理论依据。
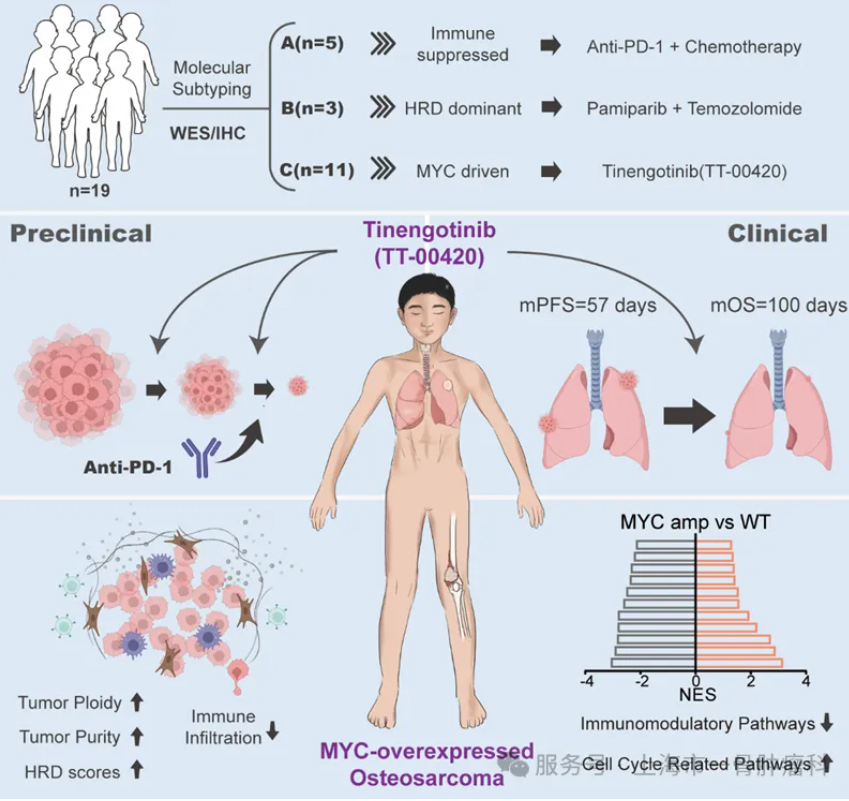
研究设计 基于本团队前期在《Nature Communications》发表的骨肉瘤分子分型研究基础,本研究设计并实施了一项前瞻性伞式临床试验。研究共纳入19例经多线治疗后复发/转移的晚期骨肉瘤患者,通过整合免疫组化(IHC)和全外显子组测序(WES)将患者精准分层至三个分子亚型指导的治疗组: S-IS亚型组(免疫抑制型):采用抗PD-1单抗联合吉西他滨和多西他赛的靶向-化疗组合方案 S-HRD亚型组(同源重组缺陷型):应用PARP抑制剂联合替莫唑胺的合成致死策略 S-MD亚型组(MYC驱动型):使用新型Aurora激酶抑制剂Tinengotinib单药靶向治疗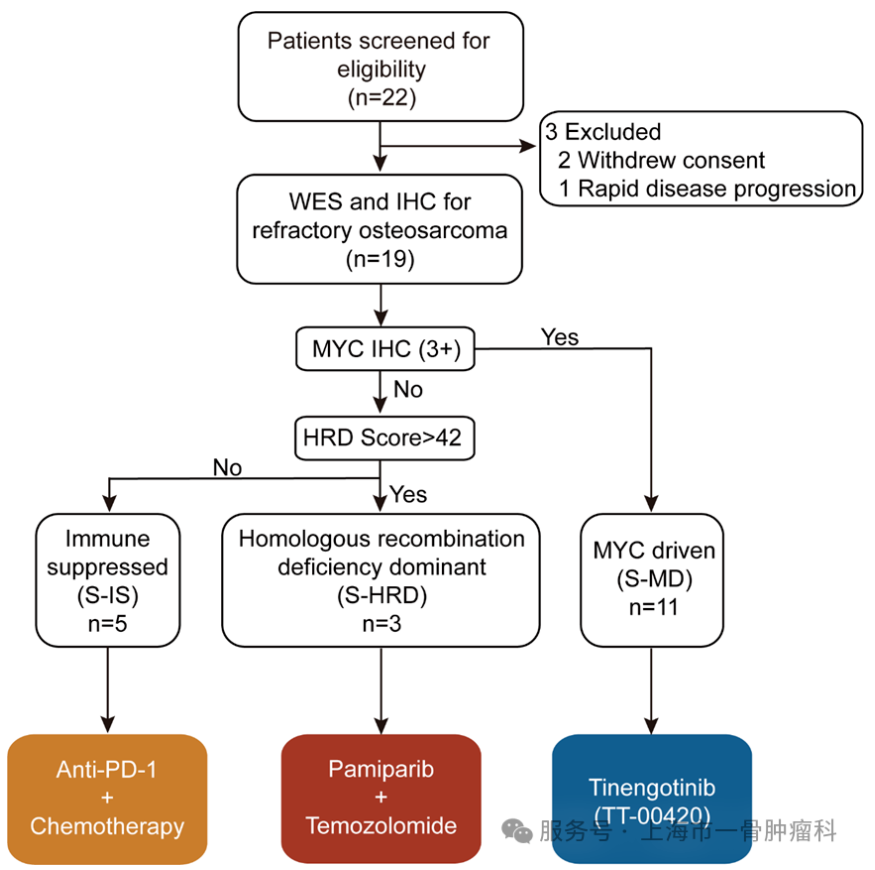
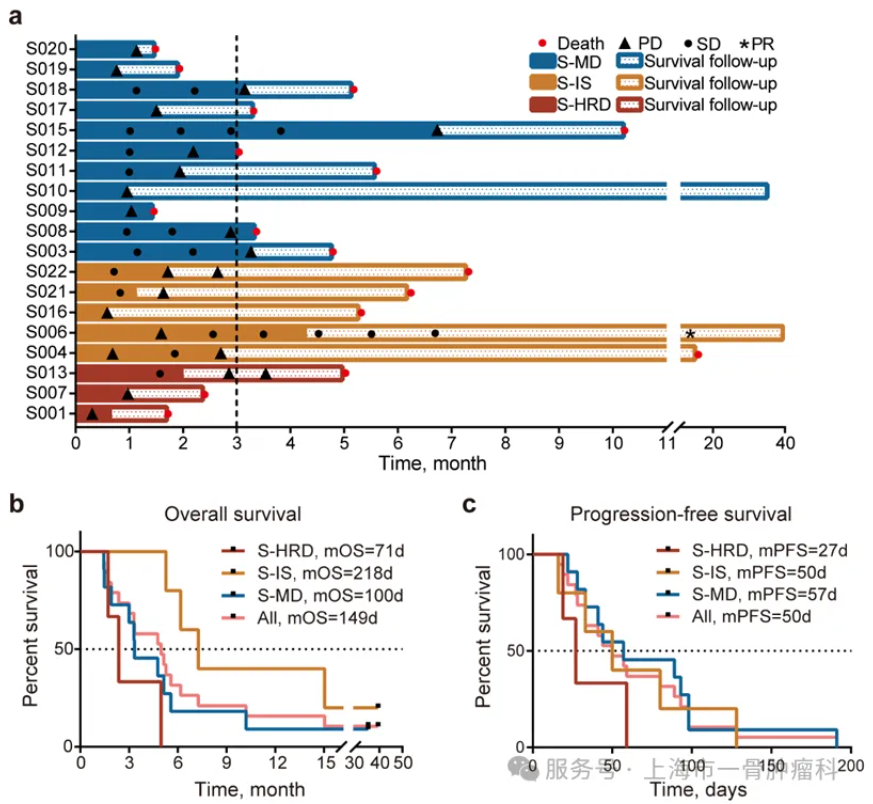
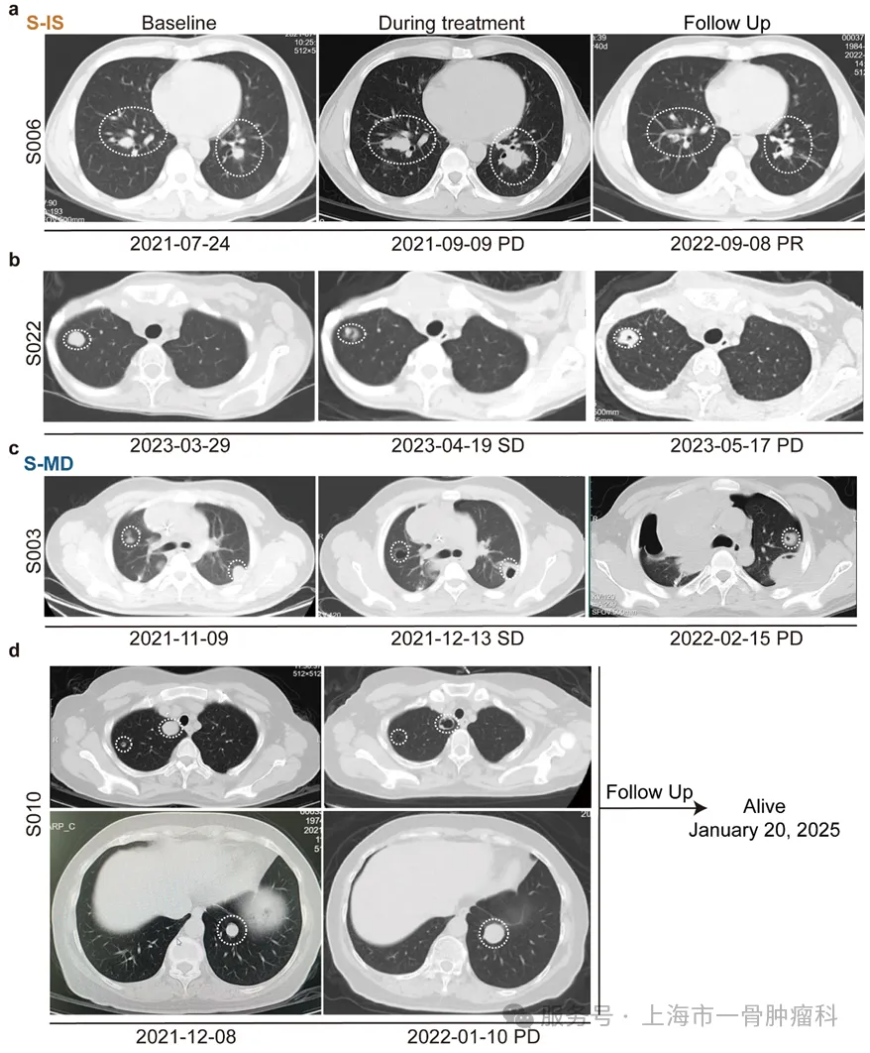
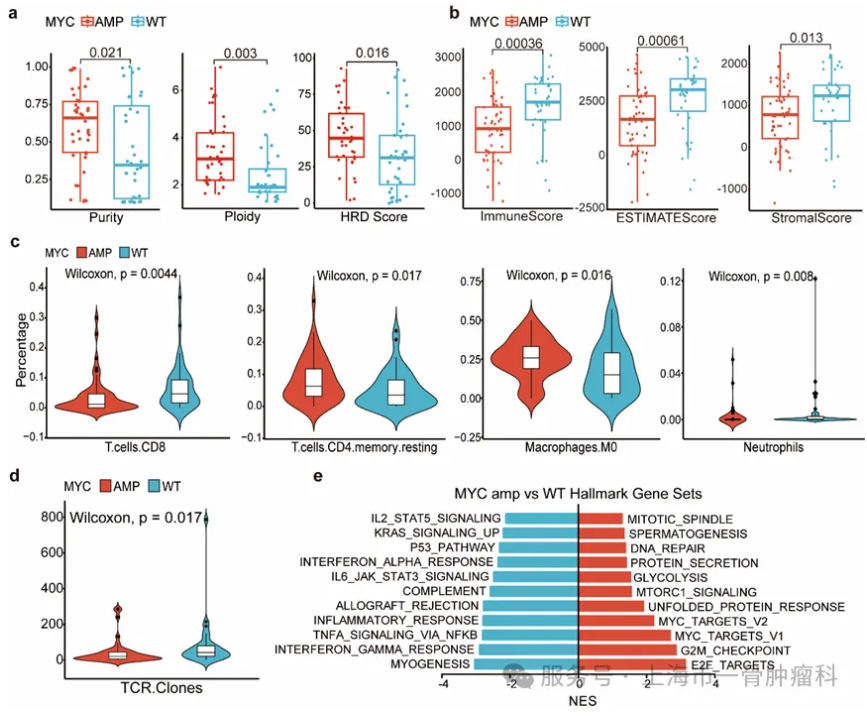
主要研究发现 1.Tinengotinib 抑制骨肉瘤生长并增强抗PD-1活性 Tinengotinib (TT-00420) 是一款处于临床试验阶段的小分子激酶抑制剂,其核心作用靶点是 Aurora A/B 激酶,展现出显著的抗癌效果。体外细胞研究结果显示,Tinengotinib可显著抑制骨肉瘤细胞增殖,并且相较于其他Aurora A和Aurora B激酶抑制剂具有更强的肿瘤抑制效果。进一步通过CDX模型和PDX模型证明了Tinengotinib抑制骨肉瘤生长并增强抗PD-1活性。 2.临床试验统计 本研究结果显示,接受不同治疗方案的患者表现出显著差异的生存获益。全组患者的中位无进展生存期(PFS)为50天(95%CI:33-89),12周时的PFS率为31.6%(95%CI:8.36-54.8)。其中,A组5例S-IS亚型患者中位PFS为50天,中位总生存期(OS)达218天。 相比之下,S-HRD亚型B组患者的治疗效果最为有限,中位PFS仅27天,中位OS为71天。在C组接受Tinengotinib治疗的11例患者中,观察到中位OS为100天(95%CI:57-167),中位PFS为57天(95%CI:33-98),12周PFS率达45.5%(95%CI:11.2-未达到)。 A组患者S004和S006均观察到延迟治疗效应,首次评估为疾病进展(PD)后在后续评估中转为疾病稳定(SD),且患者S006持续治疗后更获得部分缓解(PR)的疗效;而患者S022在治疗初期评估为SD后出现进展。 C组患者S003在接受5mg Tinengotinib治疗后首次CT评估即显示肺转移灶空洞化;患者S010在接受8mg剂量治疗1个月后,虽然两处肺转移灶显著缩小达PR标准,但因另一处病灶进展最终评估为PD,这些个案结果提示Tinengotinib对部分骨肉瘤患者的肺转移灶具有独特的抗肿瘤活性。 3.MYC扩增重塑骨肉瘤的免疫抑制微环境 本研究进一步通过上海第一人民医院骨肉瘤队列(SGH-OS)的多组学数据分析,系统揭示了MYC扩增型骨肉瘤独特的分子特征。基因组学分析显示,MYC扩增组患者更高的肿瘤纯度、肿瘤倍性和同源重组缺陷(HRD)评分,提示这类肿瘤具有更强的基因组不稳定性和克隆进化特征。 深入分析免疫微环境发现,MYC扩增型骨肉瘤呈现出典型的"免疫荒漠化"特征。免疫细胞浸润谱显示,具有抗肿瘤活性的细胞毒性CD8⁺ T细胞和中性粒细胞明显减少,而免疫抑制性的M0型巨噬细胞和静止状态的记忆CD4⁺ T细胞显著增加。T细胞受体(TCR)谱分析进一步证实,这类肿瘤的T细胞克隆多样性明显降低,表现出严重的免疫耗竭状态。 在信号通路层面,MYC扩增型骨肉瘤表现出显著的免疫抑制特征。关键的免疫调控通路如干扰素应答、炎症反应和TNFα/NF-κB信号均明显下调,而细胞增殖相关的MYC靶向通路和E2F介导的细胞周期调控通路则异常活化。 这些发现不仅揭示了MYC扩增型骨肉瘤独特的生物学特性,更为重要的是,为开发针对这一难治性亚型的精准治疗策略提供了理论依据。未来需要探索能够重塑肿瘤微环境的联合治疗策略,以克服现有的治疗瓶颈。 总 结 本研究通过整合分子分型与临床验证,为骨肉瘤精准治疗探索了新思路。研究发现基于分子亚型的个体化治疗可有效应对肿瘤异质性,其中Aurora激酶抑制剂Tinengotinib在靶向MYC驱动亚型中展现出独特潜力。虽然伞式试验设计证实了精准分型的临床价值,但患者反应的差异性也提示需要动态生物标志物监测和联合治疗优化。这项工作为突破骨肉瘤治疗瓶颈提供了重要依据,并为未来开发创新靶向策略提供了有益启示。 文献出处: Tian, K., Jiang, Y., Sun, M. et al. Targeting high-risk MYC-overexpressed osteosarcoma with an Aurora kinase inhibitor:--results from a pilot umbrella trial. npj Precis. Onc. 10, 24 (2026). https://doi.org/10.1038/s41698-025-01219-7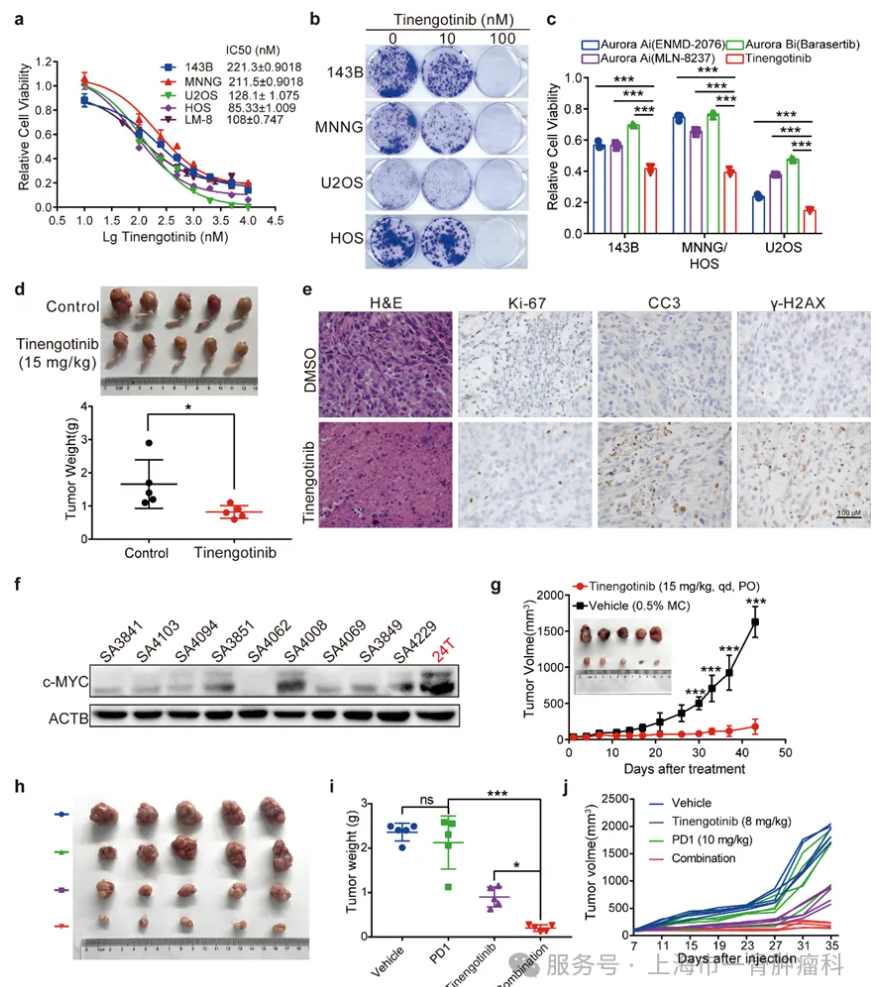


上海市徐汇区宜山东路7951号
13712345678
zhangss@yjs.edu
