新闻资讯

上海市第一人民医院骨肿瘤科领衔的多中心临床研究,为晚期软组织肉瘤患者带来了突破性希望。其研究成果近期表于国际期刊Journal for ImmunoTherapy of Cancer (IF 10.6,JCR Q1),该研究为一项溶瘤病毒OVV-01治疗晚期实体瘤的Ⅰ期、开放标签、多中心、剂量递增的安全性和耐受性研究,旨在评估OVV-01溶瘤病毒的安全性和初步疗效,临床注册号NCT04787003,通过临床试验研究首次证实了溶瘤病毒OVV-01在晚期实体瘤中的安全性,以及在晚期软组织肉瘤中的良好疗效,为肿瘤免疫治疗开辟了新的路径。

研究设计
该研究纳入了18名实体瘤患者。其中,6名软组织肉瘤(STS)患者,11例患者被纳入疗效分析;18例被纳入安全性分析。剂量递增采用3+3设计,设置四个剂量水平:6×10^7 PFU,6×10^8 PFU,6×10^9 PFU,1.2×10^11 PFU,患者每两周接受一次OVV-01瘤内注射,在首次给药3周后开始注射,共注射六剂。主要研究终点为安全性和耐受性。次要研究终点包括客观缓解率(Overall Response Rate,ORR)和疾病控制率(Disease Control Rate,DCR)。同时利用qPCR检测外周血中病毒cDNA浓度,以评估OVV-01在体内的生物分布情况。同时利用TCID50和qPCR检测患者血清、唾液、尿液及粪便样本中的病毒脱落情况。
研究结果
结果显示OVV-01瘤内注射在晚期实体瘤患者中安全且耐受性良好,未观察到剂量限制性毒性和治疗相关严重不良事件。在11名可评估疗效的患者中,客观缓解率(ORR)为27.3%,疾病控制率(DCR)为63.6%;其中4名晚期STS患者中,ORR达75%,2名实现完全缓解(CR),1名患者接受治疗后实现近三年无瘤生存,这对晚期软组织肿瘤患者是极大鼓舞。
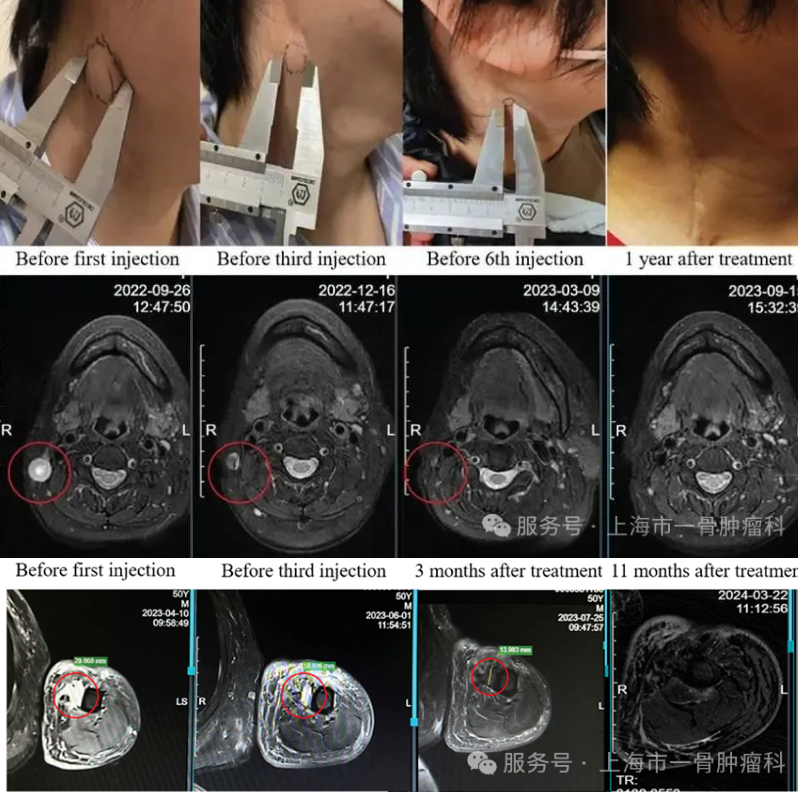
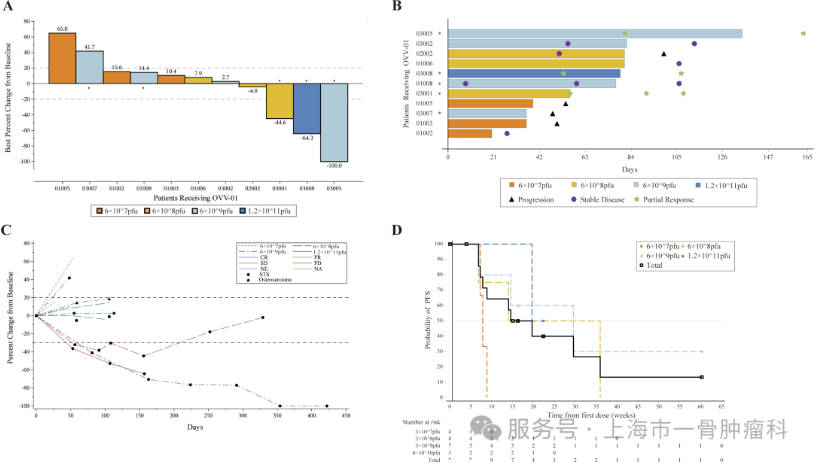
对18例患者检测OVV-01全身分布及病毒脱落情况,给药后qPCR未检出病毒基因组,但TCID50显示7例患者注射后0.25小时血清病毒水平低,且这部分患者不良反应发生率更高,所有患者唾液、尿液或粪便样本均未检出活病毒颗粒或OVV-01片段。此外检测了18例患者中抗VSV-G抗体,以评估免疫反应,给药前15例患者抗体阴性,给药后抗体滴度升高且与剂量相关,未发现抗体滴度与治疗反应明确相关。
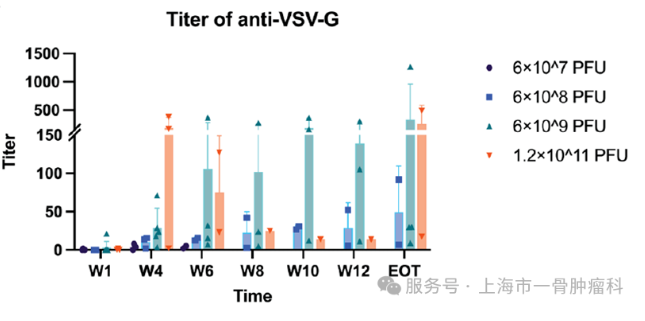
总结展望
OVV-01是携带NY - ESO - 1肿瘤抗原的重组水疱性口炎病毒(VSV),能特异性在肿瘤细胞复制、溶解细胞,释放多种抗原诱导肿瘤特异性免疫应答,以T细胞调控等方式杀伤肿瘤,有靶向精准、杀伤高效且对正常细胞损伤小的特点。
基于前期数据,其已获得美国FDA批准开展Ⅰ、Ⅱ期临床试验,国内Ⅱ期试验也已启动,由上海市一医院骨肿瘤科牵头、荣瑞医药支持、多家分中心参与,将为晚期软组织肉瘤患者带来新希望。
主要入选标准
1. 年龄≥18周岁,性别不限。
2. 经组织学/细胞学确诊为转移或复发的不可切除软组织肉瘤。
3. 至少有一个按RECIST 1.1标准判定为可测量的病灶。
4. ECOG体能状态评分为0 - 2。
5. 预计生存期不少于12周。
6. 器官和造血功能充足。
主要排除标准
1. 已知或临床怀疑有脑转移者。
2. 靶病灶2月内曾行放疗者。
3. 既往5年内患有其他活动性恶性肿瘤者。
4. 用于注射的病灶最长直径>100 mm。
5. 既往4周内参加或正在参加其他药物或医疗器械临床试验者。
6. 准备进行或既往接受过组织/器官移植者。
7. 研究期间需使用治疗性抗凝药物者。
8. 有≥3级活动性感染且具显著临床相关性者。
9. 药物未能控制的高血压、肺动脉高压或不稳定型心绞痛患者。
10. 有活动性自身免疫性疾病或有自身免疫性疾病史且可能复发者。
给药方式
OVV - 01采用瘤内注射,受试者每两周(Q2W)接受一次治疗,每两周为一个周期,给药剂量为1.2×10¹¹PFU/人,共给药6个周期。
常见不良反应
1. 注射部位反应:可能出现疼痛、肿胀、皮疹、出血或发红。
2. 流感样症状:通常表现为发烧、肌肉疼痛、疲劳、恶心、腹泻、呕吐和头痛。
3. 瘤溶解综合征:症状包括严重恶心呕吐、呼吸急促、心律不齐、肾衰竭、尿液异常、严重疲劳和/或关节疼痛等。
4. 血液学指标异常:包括淋巴细胞计数降低、白细胞计数降低、中性粒细胞计数减少、血小板计数降低、贫血等。
如果您有意愿了解该研究更详细的情况,请咨询:
上海市一骨肿瘤科:华莹奇主任专家门诊(每周五上午门诊4楼诊室)。


上海市徐汇区宜山东路7951号
13712345678
zhangss@yjs.edu
